渤健新研发的阿尔茨海默症药物被送至FDA
持续攀升的发病率,无药可医的困境,让阿尔茨海默症(AD)成了一道难以跨越的天堑,但凡有一丝研发喜讯,都会成为患者和家属的宝贵希望。最新的好消息来自美国食品和药物管理局(FDA),医药公司渤健和卫材推出的阿尔茨海默症药物将会被送至FDA的评审台,时隔17年之后,FDA会再次批准治疗阿尔茨海默症的新药吗?

新的希望
353美元,当地时间11月4日美股收盘时,渤健的股价攀升了42%,几乎是近期日均交易量的8倍,盘中一度涨至363.92美元,创下8个月以来的新高。
股价创新高的背后,是渤健在AD领域传出来的喜讯。当天,FDA在官网上公布了咨询委员会提供的背景资料。
其中,FDA审评员指出,渤健的实验性AD药物被证明有效,增加了其迅速获得批准的机会。“申请人已经提供了大量的有效性证据来支持批准”,FDA工作人员在该机构网站上发布的一份审查该药物的文件中表示。
根据安排,当地时间11月6日,由FDA召集的一个由外部专家组成的小组预计将会开会,讨论渤健和卫材公司用于治疗AD患者的阿杜卡奴抗体(Aducanumab)生物制品许可(BLA)申请,并投票决定是否向FDA推荐批准这款创新疗法。
据了解,阿杜卡奴抗体是一种与β淀粉样蛋白(β-amyloid)结合的人类单克隆抗体。它能够有选择性地与AD患者大脑中的淀粉样蛋白沉积结合,然后通过激活免疫系统,将沉积蛋白清理出大脑。主要是针对AD轻度认知障碍患者。
早在今年7月,渤健和合作伙伴卫材就向FDA提交了阿杜卡奴抗体的生物制剂上市许可申请。一个月后,FDA表示,将对两家公司的实验性AD药物阿杜卡奴抗体进行快速审查,而这也是FDA 17年来首次审查治疗这种精神疾病类药物的申请。
进入快速审查通道意味着FDA将于明年3月7日对该药物的上市批准作出决定,这比标准审查通常预期的10个月要更快。受该消息提振,渤健当天的股价截至收盘时上涨了10%。
如今,无论是即将来临的审批,还是背景文件里的初步认可,都足以让渤健兴奋不已。
值得一提的是,FDA通常会遵循咨询委员会的建议来审批药物。而在此前不久,FDA刚刚将11人外部专家咨询小组中一位持批评意见的成员驱除,该成员为梅奥诊所的临床神经病学家大卫·诺普曼博士,他的名字已经从FDA外部专家顾问预备会议上被撤下。
数据争议
不过,也不可高兴得太早,毕竟,审批流程还未开始,FDA的态度也无从明确得知。在AD药物领域,FDA一直没有松口,自2003年以来,FDA尚未批准任何有关治疗AD的新药。更何况,渤健阿杜卡奴抗体的数据还存在争议。
比如被剔除的大卫·诺普曼就对试验数据有质疑。诺普曼参与了这款药物的临床试验,上周日,他在一篇论文中写道,“阿杜卡奴单抗治疗阿尔茨海默症认知功能障碍的功效无法通过临床试验得出不同的结果”,并呼吁渤健进行另外的第三阶段试验。
除了诺普曼的质疑之外,FDA也有统计专家称渤健的分析数据存在缺陷,并不能证明阿杜卡奴抗体的有效性。
事实上,在研发路上,渤健也经历了挫折。渤健很早之前就开始了阿杜卡奴抗体的试验,2017年10月,渤健和卫材开始就这款药物的开发和商业化展开合作。
去年3月,渤健和卫材宣布,由于临床数据令人失望,他们将停止这款针对AD轻度认知障碍患者的药物的全球III期临床试验。根据渤健的说法,在分析了截至2018年12月26日的来自1748名患者的数据之后,相关研究在完成后不太可能达到预期效果。
但到了去年10月,两家公司又宣布,在与FDA讨论并进一步分析更大量的数据之后,他们将寻求对该药物的监管批准。
即便有过失败的经历,即便临床数据仍然无法让所有审查者满意,但渤健的进展仍然让外界看到了一丝希望,华尔街已经用实际行动表明了态度。富国证券分析师Jim Birchenough表示,尽管FDA的最终结果难以预测,但相信会议上将会有更多积极的建议,预计周五的咨询委员会将建议批准通过该新药,并将渤健评级由“持有”上调至“买入”,同时将其目标价上调至390美元。
难在哪
FDA短短的几个字,就让渤健的股价飙升了40%,也扭转了华尔街的态度,足见市场对于AD药物的期待。
国际阿尔茨海默症协会发布的《2018年世界阿尔茨海默症报告》显示,截至2018年,全球共有5000万AD患者,社会相关成本达1万亿美元,而随着人口老龄化的趋势,预计到2030年全球AD患者将会达到8200万人,2050年将达到1.52亿人。
“从西医的逻辑讲,必须清晰病理机制,然后有与之相对应的药理,达到治疗目的。如果病理机制清晰,获批还是有可能的。”中国中医科学院中医学副教授孙海舒指出。
不过,由于AD发病机制尚未明确,现有药物均只能缓解临床症状,改善或逆转AD进程的药物尚未出现。“阿尔茨海默症很难真正治愈,其诱因可能有多种,还有适应症的问题,最多只能是延缓。”医疗战略咨询公司LatitudeHealth创始人赵衡坦言。
抗体药物研发总监闫闰告诉北京商报记者,阿尔兹海默症的发病机制至今没有定论。之前多年此研究领域倾向于认为beta-amyloid是致病根源,但是随着针对减少beta-amyloid产生的临床药物相继折戟,学界业界也开始重新审视此理论。而如果连发病机制都无法确定,开发治疗药物就更难上加难了。
除了上述原因以外,闫闰还提到了其他因素,包括科研模型和临床标准等等。以临床标准为例,闫闰称,早期FDA的临床药效判定标准是对认知能力和记忆的改善。但早期阿尔兹海默症患者并没有这两个方面的表现,而晚期的重症患者如果药物效果不够强又很难展示出药物的疗效,从而造成大量药物在临床阶段折戟。FDA已经调整判定标准,把biomarker的改变纳入判断标准。但biomarker本身的确定和检测又是一个难点。
此外,闫闰还指出,神经类疾病是传统难攻的领域,因为血脑屏障的存在,以及大脑自有的独特免疫系统,中枢神经系统疾病一直是药物研发的困难领域。随着对大脑的深入研究,也慢慢展示出大脑各区域的异质性,每个功能区域对药物响应可能不同,也就加大了系统治疗的难度。
据了解,目前全球获批用于临床治疗的药物只有5款,即多奈哌齐、卡巴拉汀、加兰他敏、美金刚以及多奈哌齐+美金刚复方制剂。不过,这些药物主要作用机制为胆碱酯酶抑制剂或NMDA拮抗剂,只能达到改善脑血流量,促进脑认知功能恢复的作用,无法彻底根治老年痴呆。
不是没有药企努力过。在过去20多年来,全球各大制药公司相继投入了数千亿美元研发药物,美国药品研究与制造商协会2018年发布的报告指出,在1998-2017年期间,全球已有146个AD药物在临床中遭遇失败,仅有4个药物成功上市;同时,几乎所有靶向β-淀粉样蛋白的治疗策略在临床试验中也全军覆没。AD新药研发失败率高达99.6%。
赵衡表示,“大家认为这个市场很大,也在持续投入,但总体上来看,没有龙头药物,且新药的失败率太高了”。
去年3月,渤健宣布终止临床试验之后,大多数研究人员和生物技术公司的高管都认为,尽管阿尔茨海默症的病例在不断增加,但他们几乎看不到任何希望能够研制出一种能够帮助患者的药物。
因此,阿杜卡奴抗体一度被认为是阿尔茨海默症最后的希望。对于相关的实验数据、审批流程等情况,北京商报记者联系了渤健方面,不过截至发稿还未收到回复。
值得一提的是,除了阿杜卡奴抗体,去年11月,由上海药物研究所和上海绿谷制药累计投入4亿美元共同研发的阿尔茨海默症原创新药——“九期一”甘露特钠胶囊(GV-971)获得中国国家药品监督管理局有条件批准,并在国内正式上市。该药物用于轻度至中度阿尔茨海默症,改善患者认知功能。今年4月,FDA批准“九期一”开始在北美、欧盟等地开展临床试验,预计2024年完成。
标签: 渤健
-
 天津知识产权保护体系进一步完善 高效益加快知识产权价值实现 市政府新闻办昨天召开新闻发布会,发布《2021年天津市知识产权发展状况白皮书》和《2021年天津市知识产权保护状况白皮书》。记者从发布会上
天津知识产权保护体系进一步完善 高效益加快知识产权价值实现 市政府新闻办昨天召开新闻发布会,发布《2021年天津市知识产权发展状况白皮书》和《2021年天津市知识产权保护状况白皮书》。记者从发布会上 -
 下调金融机构外汇存款准备金率 提升金融机构外汇资金运用能力 据央行网站4月25日晚间消息,为提升金融机构外汇资金运用能力,中国人民银行决定,自2022年5月15日起,下调金融机构外汇存款准备金率1个百
下调金融机构外汇存款准备金率 提升金融机构外汇资金运用能力 据央行网站4月25日晚间消息,为提升金融机构外汇资金运用能力,中国人民银行决定,自2022年5月15日起,下调金融机构外汇存款准备金率1个百 -
 钢铁行业受供给约束成本持续上升 提高经济效益难度增大 今年一季度,中国钢铁行业受供给约束、需求收缩、成本上升等因素影响,营收利润出现下降。4月25日,中国钢铁工业协会举行2022年一季度信息
钢铁行业受供给约束成本持续上升 提高经济效益难度增大 今年一季度,中国钢铁行业受供给约束、需求收缩、成本上升等因素影响,营收利润出现下降。4月25日,中国钢铁工业协会举行2022年一季度信息 -
 完美世界高开高走 公司游戏研发升级转型已见成效 4月26日早盘,完美世界高开高走。截至发稿已封死涨停,涨停板封单接近25万手之巨。消息面,4月25日晚间完美世界发布2021年年报及2022年第一
完美世界高开高走 公司游戏研发升级转型已见成效 4月26日早盘,完美世界高开高走。截至发稿已封死涨停,涨停板封单接近25万手之巨。消息面,4月25日晚间完美世界发布2021年年报及2022年第一 -
 北京商超通过产地直采调货机制紧急增加货量 保障市场供应稳定 面对突发的疫情,北京各大商超企业迅速开启了保供模式。4月24日,北京商报记者从多家商超企业了解到,针对北京市突发局部疫情,多家超市企
北京商超通过产地直采调货机制紧急增加货量 保障市场供应稳定 面对突发的疫情,北京各大商超企业迅速开启了保供模式。4月24日,北京商报记者从多家商超企业了解到,针对北京市突发局部疫情,多家超市企 -
 农村“一刻钟”建模 一体化县域商业网络体系升级 北京的便民商业网点建设已从市区延伸到郊区。4月24日,北京商报记者从北京市商务局了解到,北京农村地区便民商业网点改造提升典型示范类项
农村“一刻钟”建模 一体化县域商业网络体系升级 北京的便民商业网点建设已从市区延伸到郊区。4月24日,北京商报记者从北京市商务局了解到,北京农村地区便民商业网点改造提升典型示范类项
-
 传祺影豹惊艳不止一点,造型设计再获权威认证 4月26日,中央广播电视总台·2021中国汽车风云盛典颁奖典礼在京拉开序幕。参加本次盛典候选名单的车型有近一千款优秀汽车产品,不乏包括2021
传祺影豹惊艳不止一点,造型设计再获权威认证 4月26日,中央广播电视总台·2021中国汽车风云盛典颁奖典礼在京拉开序幕。参加本次盛典候选名单的车型有近一千款优秀汽车产品,不乏包括2021 -
 近8万师生挤爆直播间,毓婷学院奖创意课堂全国场火热开讲! 3月29日到4月26日毓婷携手学院奖,开启10场线上巡讲来自北京、天津、河南、山西内蒙、甘肃、山东、上海、安徽辽宁、云南、广东等27个省市的
近8万师生挤爆直播间,毓婷学院奖创意课堂全国场火热开讲! 3月29日到4月26日毓婷携手学院奖,开启10场线上巡讲来自北京、天津、河南、山西内蒙、甘肃、山东、上海、安徽辽宁、云南、广东等27个省市的 - 崔东树:以A00级产品切入新能源乘用车,曙光汽车未来可期 新能源汽车被公认为全球汽车产业唯一可见的未来发展方向。在各国加速新能源产业布局的基础上,中国新能源汽车市场呈现出量级增长的态势,包
-
 圣奥化学加入“携手可持续发展”(TfS)倡议 4月27日,全球性倡议组织携手可持续发展(Together for Sustainability,简称TfS)宣布,圣奥化学科技有限公司(简称圣奥化学)正式加入Tf
圣奥化学加入“携手可持续发展”(TfS)倡议 4月27日,全球性倡议组织携手可持续发展(Together for Sustainability,简称TfS)宣布,圣奥化学科技有限公司(简称圣奥化学)正式加入Tf - 菜鸟在北京封控区推24小时配送 记者从菜鸟了解到,该物流企业在京运力将向封控区和管控区做一定倾斜,优先保证这些风险区域的消费者及时收货。目前菜鸟已在封控区推出24小
-
 【正式启用】| 汇聚行业资源·打造共赢的义乌市跨境电商服务中心劲爆来袭 目前,义乌市跨境电商综合服务中心(以下简称服务中心)已正式启用。义乌是一座建在市场上的城市,每天,有数十万名中外客商在这里洽谈生意
【正式启用】| 汇聚行业资源·打造共赢的义乌市跨境电商服务中心劲爆来袭 目前,义乌市跨境电商综合服务中心(以下简称服务中心)已正式启用。义乌是一座建在市场上的城市,每天,有数十万名中外客商在这里洽谈生意 -
 Lavinia | 重回自然,浪漫繁花 随着自然危机的加深,环保口号的声音也越来越多,人与自然,科技与自然成为各行各业研究的方向。Lavinia2022夏季的新品系列,也大量的采用
Lavinia | 重回自然,浪漫繁花 随着自然危机的加深,环保口号的声音也越来越多,人与自然,科技与自然成为各行各业研究的方向。Lavinia2022夏季的新品系列,也大量的采用 - 协助解除弹窗、分发物资 北京链家志愿者加入潘家园、劲松防疫 近日,北京市朝阳区潘家园街道、劲松街道等地成为重点防疫区域。作为房产经纪人志愿者,北京链家志愿者们纷纷加入社区防疫队伍,在携手抗击
-
 深睡为夺冠蓄能!顾家家居首批顾家深睡床垫交付亚运村! 亚运的脚步越来越近,56个竞赛场馆都已竣工验收,亚运村也进入装修扫尾工作,坐落于钱塘江南岸的杭州亚运村,赛时将为各国运动员、随队官员
深睡为夺冠蓄能!顾家家居首批顾家深睡床垫交付亚运村! 亚运的脚步越来越近,56个竞赛场馆都已竣工验收,亚运村也进入装修扫尾工作,坐落于钱塘江南岸的杭州亚运村,赛时将为各国运动员、随队官员 -
 美呀植牙史竞医术高超,仁医仁术赢口碑 美呀植牙是国内领先的全国口腔连锁机构,专注口腔种植领域,目前在全国一二线城市19城建立26家自营门诊。从成立之初,美呀植牙就以让所有老
美呀植牙史竞医术高超,仁医仁术赢口碑 美呀植牙是国内领先的全国口腔连锁机构,专注口腔种植领域,目前在全国一二线城市19城建立26家自营门诊。从成立之初,美呀植牙就以让所有老 - 元道经纬相机六周年,引领全行业现场拍照 4月27日,元道经纬相机上线六周年之际,重磅发布了致所有用户的一封信,信中既展示了这六年来的成绩单,也向所有用户讲述了六年来的的成长
-
 服务企业更好出海,大龙网携手欧中跨境电商协会举办欧盟法律专场培训会 4月20日,由欧中跨境电商协会主办,联合荷兰凯拓国际律师事务所,成功举办了以商业合同和产品合规性为主题的线上欧洲法律专场培训会。培训
服务企业更好出海,大龙网携手欧中跨境电商协会举办欧盟法律专场培训会 4月20日,由欧中跨境电商协会主办,联合荷兰凯拓国际律师事务所,成功举办了以商业合同和产品合规性为主题的线上欧洲法律专场培训会。培训 - 顾家家居推出79800套餐有市场吗?艾瑞咨询报告或许给出了答案 整家或者全屋定制套餐,是否只能走客单均价2~3万元的绝对性价比路线?相信很多人都有这种想法,笔者本人也曾经这样认为。但仔细一想,这种
-
 上海保供有一条“助老通道”,20天为2万老人送达生活物资 疫情期间,物流运力紧张,保供压力大。而面对老年人这一特殊群体,他们不擅长使用手机网购,有些高龄老人长期住在养老院,需要稳定的食品营养补
上海保供有一条“助老通道”,20天为2万老人送达生活物资 疫情期间,物流运力紧张,保供压力大。而面对老年人这一特殊群体,他们不擅长使用手机网购,有些高龄老人长期住在养老院,需要稳定的食品营养补 - 首个通过GCP功效验证的冲牙器品牌!倍至推动口腔护理行业走进专业化时代 从1922年中国第一支牙膏——三星牙膏诞生,开启本土牙膏业的发展,到如今各式各样的牙膏、漱口水、口腔喷雾、牙贴、口腔爆珠等产品百花...
-
 美丽岸,西雅图现房海景公寓,享尽太平洋艾略特湾之美 美亚置业西雅图海景现房公寓,THE EMERALD 美丽岸,享尽太平洋艾略特湾之美就像西雅图市中心天际线上的一颗宝石,高达40层的西雅图现房海
美丽岸,西雅图现房海景公寓,享尽太平洋艾略特湾之美 美亚置业西雅图海景现房公寓,THE EMERALD 美丽岸,享尽太平洋艾略特湾之美就像西雅图市中心天际线上的一颗宝石,高达40层的西雅图现房海 -
 知名数字资产交易平台8V与Onramper达成合作,强强赋能OTC业务 近日,知名元宇宙生态数字资产交易平台8V隆重宣布与全球领先的OTC服务商Onramper达成战略合作,完了技术对接并正式上线OTC业务。此次合作带来
知名数字资产交易平台8V与Onramper达成合作,强强赋能OTC业务 近日,知名元宇宙生态数字资产交易平台8V隆重宣布与全球领先的OTC服务商Onramper达成战略合作,完了技术对接并正式上线OTC业务。此次合作带来 -
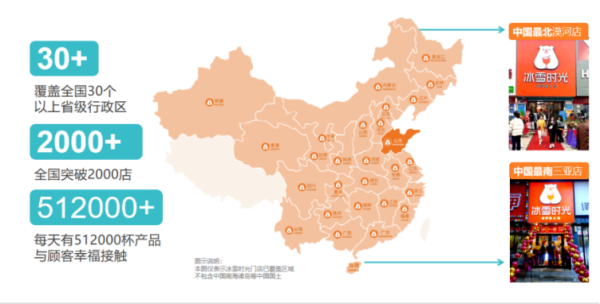 奶茶行业品牌多、竞争大 冰雪时光靠什么赢得掌声? 随着头部品牌的下沉,新式茶饮行业竞争愈发激烈。为了抢占更多市场份额,各大高端茶饮品牌不断拓宽价格带,纷纷推出平价系列产品。即便如此
奶茶行业品牌多、竞争大 冰雪时光靠什么赢得掌声? 随着头部品牌的下沉,新式茶饮行业竞争愈发激烈。为了抢占更多市场份额,各大高端茶饮品牌不断拓宽价格带,纷纷推出平价系列产品。即便如此 -
 原料新鲜 用料扎实 冰雪时光稳扎茶饮下沉市场 近些年来,随着人们生活水平的提高,美团、饿了么等外卖平台盛行,新式茶饮行业迎来快速发展。数据显示,我国在业 存续奶茶相关企业已经达
原料新鲜 用料扎实 冰雪时光稳扎茶饮下沉市场 近些年来,随着人们生活水平的提高,美团、饿了么等外卖平台盛行,新式茶饮行业迎来快速发展。数据显示,我国在业 存续奶茶相关企业已经达 - 住建部科技示范“立体园林绿色建筑”健康中国创意城市在京签约 视日前,住建部科技项目立体园林绿色建筑与健康中国创意城市示范工程合作签约仪式在住建部科技与产业化发展中心举行。住建部科技与产业化发
-
 洪森总理会见太子集团董事长陈志 昨日,洪森总理在和平大厦会见太子集团控股陈志公爵率领的从事矿业、房地产、贸易,物流和证券的投资企业代表。此次访问还反映了陈志公爵和
洪森总理会见太子集团董事长陈志 昨日,洪森总理在和平大厦会见太子集团控股陈志公爵率领的从事矿业、房地产、贸易,物流和证券的投资企业代表。此次访问还反映了陈志公爵和 - 蜜雪冰城:攻守结合 知产保护走在前 你爱我呀我爱你,蜜雪冰城甜蜜蜜……这首歌传遍大街小巷。气温升高,来杯蜜雪冰城的柠檬水,再惬意不过。近年来,蜜雪冰城深耕下沉市场...
-
 岚图FREE实力登顶 东风公司斩获中央广播电视总台·2021中国汽车风云盛典四项大奖 4月26日,由中央广播电视总台主办、总台财经节目中心特别策划的中央广播电视总台·2021中国汽车风云盛典落下帷幕。凭借过硬实力,东风汽车
岚图FREE实力登顶 东风公司斩获中央广播电视总台·2021中国汽车风云盛典四项大奖 4月26日,由中央广播电视总台主办、总台财经节目中心特别策划的中央广播电视总台·2021中国汽车风云盛典落下帷幕。凭借过硬实力,东风汽车 -
 广州加拿达外国语学校——“双出口”给孩子更多选择 很多家长在选择学校时,都有一个需求,他们希望孩子有一个双出口,在高中阶段升学时,既可以走国内升学之路,也可以走国际教育之路。双出口留给
广州加拿达外国语学校——“双出口”给孩子更多选择 很多家长在选择学校时,都有一个需求,他们希望孩子有一个双出口,在高中阶段升学时,既可以走国内升学之路,也可以走国际教育之路。双出口留给 -
 INOT1发行新专辑《冲天志》NUMBER K COMPANY参与制作 最近INOT1用中文和英文发行了包含主打歌一杯火焰在内的新专辑《冲天之志》, 受到广大粉丝的热烈欢迎。据悉,参与制作INTO1出道专辑的NUMBE
INOT1发行新专辑《冲天志》NUMBER K COMPANY参与制作 最近INOT1用中文和英文发行了包含主打歌一杯火焰在内的新专辑《冲天之志》, 受到广大粉丝的热烈欢迎。据悉,参与制作INTO1出道专辑的NUMBE - 盈康生命财报暗藏转机,聪明资金增持 4月25日,盈康生命科技股份有限公司(简称:盈康生命,代码:300143 SZ)发布业绩预告,预计2021年营业收入实现110,000万元,重组前口径同
-
 外汇天眼:外汇交易中出金有问题,如何正确维权? 关注外汇天眼的投资者一定经常到天眼君发布《成功到账》系列的文章,在这些文章中遭遇了外汇出金问题的投资者都如愿拿到了自己被拖延的资金
外汇天眼:外汇交易中出金有问题,如何正确维权? 关注外汇天眼的投资者一定经常到天眼君发布《成功到账》系列的文章,在这些文章中遭遇了外汇出金问题的投资者都如愿拿到了自己被拖延的资金 -
 弥玥泉喷雾丨妈生好皮的底妆秘诀,终于跟化妆师学会了 阳光正好,微风不燥,一颗疯狂想外出的心早就按捺不住了,这样的好天气,不化个美美的妆、约个三五好友赏花看景,简直就是辜负好时光呀!不过,对
弥玥泉喷雾丨妈生好皮的底妆秘诀,终于跟化妆师学会了 阳光正好,微风不燥,一颗疯狂想外出的心早就按捺不住了,这样的好天气,不化个美美的妆、约个三五好友赏花看景,简直就是辜负好时光呀!不过,对 -
 2022广州从化区幼儿园报名 小区从化户籍业主子女报名时间公布 ➤小区配套幼儿园从化户籍业主子女报名时间:4月28日至30日上午9:00-12:00,下午14:30-17:30注:小区从化户籍业主子女报名时间,符合条件的
2022广州从化区幼儿园报名 小区从化户籍业主子女报名时间公布 ➤小区配套幼儿园从化户籍业主子女报名时间:4月28日至30日上午9:00-12:00,下午14:30-17:30注:小区从化户籍业主子女报名时间,符合条件的 -
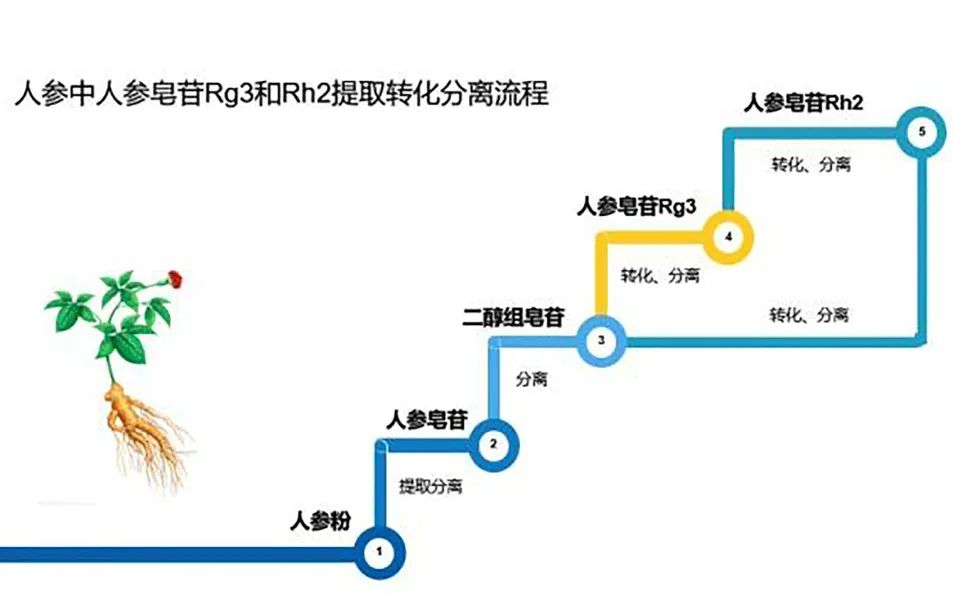 安普胶囊人参皂苷产品,抗癌修复、增强免疫的天然护命素! 人参自古即有「百草之王」之称,居中国四大补品之首,一直以来都备受推崇。其主要有大补元气,安神益智、复脉固脱,补脾益肺,生津止渴等来
安普胶囊人参皂苷产品,抗癌修复、增强免疫的天然护命素! 人参自古即有「百草之王」之称,居中国四大补品之首,一直以来都备受推崇。其主要有大补元气,安神益智、复脉固脱,补脾益肺,生津止渴等来 -
 天津知识产权保护体系进一步完善 高效益加快知识产权价值实现 市政府新闻办昨天召开新闻发布会,发布《2021年天津市知识产权发展状况白皮书》和《2021年天津市知识产权保护状况白皮书》。记者从发布会上
天津知识产权保护体系进一步完善 高效益加快知识产权价值实现 市政府新闻办昨天召开新闻发布会,发布《2021年天津市知识产权发展状况白皮书》和《2021年天津市知识产权保护状况白皮书》。记者从发布会上 -
 从安全相识到牵手奔现 爱聊阐释了线上社交的四个阶段 近日,由于疫情的原因,许多小情侣见不到面,被迫开启了网恋模式,也正因如此,关于线上交友的问题,也成为了我们茶余饭后的谈资。一位在爱聊APP
从安全相识到牵手奔现 爱聊阐释了线上社交的四个阶段 近日,由于疫情的原因,许多小情侣见不到面,被迫开启了网恋模式,也正因如此,关于线上交友的问题,也成为了我们茶余饭后的谈资。一位在爱聊APP -
 下调金融机构外汇存款准备金率 提升金融机构外汇资金运用能力 据央行网站4月25日晚间消息,为提升金融机构外汇资金运用能力,中国人民银行决定,自2022年5月15日起,下调金融机构外汇存款准备金率1个百
下调金融机构外汇存款准备金率 提升金融机构外汇资金运用能力 据央行网站4月25日晚间消息,为提升金融机构外汇资金运用能力,中国人民银行决定,自2022年5月15日起,下调金融机构外汇存款准备金率1个百 -
 蝶适-DISC,让近视青少年拥有光明未来 近日,越发受到关注的青少年近视防控问题有了最新的成果研究,蝶适-DISC的出现,大放光彩,被有些消费者称之为划时代的新突破,给万千青少
蝶适-DISC,让近视青少年拥有光明未来 近日,越发受到关注的青少年近视防控问题有了最新的成果研究,蝶适-DISC的出现,大放光彩,被有些消费者称之为划时代的新突破,给万千青少 -
 《现在就告白5》,爱情和爱好不能并存吗? 她喜欢宠物,于是养了一屋子爬宠;他因少时被蛇咬过,所以一直对于爬宠敬而远之。有一天,她与他相遇。在一起半年后,她主动告知关于爬宠的
《现在就告白5》,爱情和爱好不能并存吗? 她喜欢宠物,于是养了一屋子爬宠;他因少时被蛇咬过,所以一直对于爬宠敬而远之。有一天,她与他相遇。在一起半年后,她主动告知关于爬宠的 -
 钢铁行业受供给约束成本持续上升 提高经济效益难度增大 今年一季度,中国钢铁行业受供给约束、需求收缩、成本上升等因素影响,营收利润出现下降。4月25日,中国钢铁工业协会举行2022年一季度信息
钢铁行业受供给约束成本持续上升 提高经济效益难度增大 今年一季度,中国钢铁行业受供给约束、需求收缩、成本上升等因素影响,营收利润出现下降。4月25日,中国钢铁工业协会举行2022年一季度信息 -
 完美世界高开高走 公司游戏研发升级转型已见成效 4月26日早盘,完美世界高开高走。截至发稿已封死涨停,涨停板封单接近25万手之巨。消息面,4月25日晚间完美世界发布2021年年报及2022年第一
完美世界高开高走 公司游戏研发升级转型已见成效 4月26日早盘,完美世界高开高走。截至发稿已封死涨停,涨停板封单接近25万手之巨。消息面,4月25日晚间完美世界发布2021年年报及2022年第一 -
 同花顺早盘大幅走低 一季度市场行情波动较大 4月26日,同花顺早盘大幅走低,一度跌超13%,报76 3元,跌超10%。4月25日,同花顺披露2022年第一季度报告,公司实现营业收入5 15亿元,同比
同花顺早盘大幅走低 一季度市场行情波动较大 4月26日,同花顺早盘大幅走低,一度跌超13%,报76 3元,跌超10%。4月25日,同花顺披露2022年第一季度报告,公司实现营业收入5 15亿元,同比 -
 药明康德强势反弹 规模效应得以进一步显现 4月26日早盘,药明康德强势反弹。截至发稿报101 56元,涨3 87%,已将昨日跌幅全部收回。消息面,4月25日晚间,药明康德披露一季报,公司实
药明康德强势反弹 规模效应得以进一步显现 4月26日早盘,药明康德强势反弹。截至发稿报101 56元,涨3 87%,已将昨日跌幅全部收回。消息面,4月25日晚间,药明康德披露一季报,公司实 -
 4月以来各大指数继续震荡下跌 医药龙头股恒瑞医药开盘即暴跌 今日(26日)早盘,A股三大股指集体高开,沪指涨0 07%,深证成指涨0 22%,创业板涨0 17%。4月25日,上证指数跌破3000点,96%以上个股下跌。在
4月以来各大指数继续震荡下跌 医药龙头股恒瑞医药开盘即暴跌 今日(26日)早盘,A股三大股指集体高开,沪指涨0 07%,深证成指涨0 22%,创业板涨0 17%。4月25日,上证指数跌破3000点,96%以上个股下跌。在 - 远东股份:子公司圣达电气失控不再并表,原总经理李民被刑事立案 远东股份(3 580, -0 19, -5 04%)昨晚公告,控股子公司圣达电气有限公司(以下简称圣达电气)原法定代表人、董事、总经理(已解除劳动关系)李
-
 华润万家以变化的姿态拥抱“可持续” 在第53个世界地球日到来时,始终致力于引领消费升级,共创美好生活的华润万家,将可持续理念融入到日常经营管理中,坚持探讨更多绿色行动,
华润万家以变化的姿态拥抱“可持续” 在第53个世界地球日到来时,始终致力于引领消费升级,共创美好生活的华润万家,将可持续理念融入到日常经营管理中,坚持探讨更多绿色行动, -
 沪指跌破3000点关口后再次跌破2900点 市场担忧情绪再起 4月25日,沪指跌破3000点关口,4月26日开盘,再次跌破2900点,市场担忧情绪再起。作为资本市场的重要长期投资者及压舱石,险资对未来市场怎
沪指跌破3000点关口后再次跌破2900点 市场担忧情绪再起 4月25日,沪指跌破3000点关口,4月26日开盘,再次跌破2900点,市场担忧情绪再起。作为资本市场的重要长期投资者及压舱石,险资对未来市场怎 -
 A股大盘跌破2900点 市场担忧情绪进一步升温 每次跌破3000点之后抄底的,之后基本都是赢家。看着上证指数一度跌破2900点后反弹,深圳一位私募人士向第一财经记者表示。虽然上证指数多年
A股大盘跌破2900点 市场担忧情绪进一步升温 每次跌破3000点之后抄底的,之后基本都是赢家。看着上证指数一度跌破2900点后反弹,深圳一位私募人士向第一财经记者表示。虽然上证指数多年 -
 A股全线飘绿三大股指均收跌逾5% 沪指失守3000点 4月25日,A股全线飘绿,三大股指均收跌逾5%,其中沪指失守3000点,最低下探至2928 51点,系自2020年6月19日以来的指数新低。深证成指收跌6
A股全线飘绿三大股指均收跌逾5% 沪指失守3000点 4月25日,A股全线飘绿,三大股指均收跌逾5%,其中沪指失守3000点,最低下探至2928 51点,系自2020年6月19日以来的指数新低。深证成指收跌6 -
 多个奢侈品牌宣布提价 奢侈品本身不具备真正的投资价值 近期,多个奢侈品牌宣布提价,奢侈品市场涨声一片。在奢侈品保值增值预期下,一些消费者受到刺激,动起了投资的念头。分析人士提醒,奢侈品
多个奢侈品牌宣布提价 奢侈品本身不具备真正的投资价值 近期,多个奢侈品牌宣布提价,奢侈品市场涨声一片。在奢侈品保值增值预期下,一些消费者受到刺激,动起了投资的念头。分析人士提醒,奢侈品 -
 十几元钱的奶茶,冰雪时光是怎么做到好喝又高级的? 随着消费的不断升级,近几年新式茶饮店也如雨后春笋般的崛起,街边随处可见各种品牌的茶饮店铺。消费者也从最开始的单纯追求口感,到现在健
十几元钱的奶茶,冰雪时光是怎么做到好喝又高级的? 随着消费的不断升级,近几年新式茶饮店也如雨后春笋般的崛起,街边随处可见各种品牌的茶饮店铺。消费者也从最开始的单纯追求口感,到现在健 -
 北京丰台全力保障居民“菜篮子” 新发地蔬菜交易市场有序进行 为做好保供稳价工作,北京市丰台区今天启动点对点补货机制,第一时间发动新发地、岳各庄两大批发市场,做好货源组织工作,协调加快保供车辆
北京丰台全力保障居民“菜篮子” 新发地蔬菜交易市场有序进行 为做好保供稳价工作,北京市丰台区今天启动点对点补货机制,第一时间发动新发地、岳各庄两大批发市场,做好货源组织工作,协调加快保供车辆 -
 伊施以勒签约“创世纪-米开朗基罗”进军中国数字藏品市场 作为元宇宙的重要应用方式,数字藏品市场短期内在我国爆发式增长,成为文旅行业广泛关注的焦点。作为国际顶级IP的创世纪-米开朗基罗,近日
伊施以勒签约“创世纪-米开朗基罗”进军中国数字藏品市场 作为元宇宙的重要应用方式,数字藏品市场短期内在我国爆发式增长,成为文旅行业广泛关注的焦点。作为国际顶级IP的创世纪-米开朗基罗,近日 -
 “土货”成为抢手“网货” 秀山县大力发展农村电商产业 长久以来,物流产品人才是制约农村电商发展的三大难题。重庆秀山县以构建城乡双向物流、打造电商产业扶贫基地、开展电商培训等手段破解难题
“土货”成为抢手“网货” 秀山县大力发展农村电商产业 长久以来,物流产品人才是制约农村电商发展的三大难题。重庆秀山县以构建城乡双向物流、打造电商产业扶贫基地、开展电商培训等手段破解难题
热门资讯
-
 知名数字资产交易平台8V与Onramper达成合作,强强赋能OTC业务 近日,知名元宇宙生态数字资产交易...
知名数字资产交易平台8V与Onramper达成合作,强强赋能OTC业务 近日,知名元宇宙生态数字资产交易... -
 外汇天眼:外汇交易中出金有问题,如何正确维权? 关注外汇天眼的投资者一定经常到天...
外汇天眼:外汇交易中出金有问题,如何正确维权? 关注外汇天眼的投资者一定经常到天... -
 健康饮食需求激增!DROODS道得富以健康食品助力改善国民健康水平 自健康中国战略实施以来,人民群众...
健康饮食需求激增!DROODS道得富以健康食品助力改善国民健康水平 自健康中国战略实施以来,人民群众... -
 常州京城皮肤病医院樊战军:为什么很多皮肤病夜间觉得瘙痒 有皮肤病的友友们有没有觉得很疑惑...
常州京城皮肤病医院樊战军:为什么很多皮肤病夜间觉得瘙痒 有皮肤病的友友们有没有觉得很疑惑...
观察
图片新闻
-
 山东开展药品经营专项检查 及时排查和化解风险隐患 日前,山东省药品监督管理局印发《...
山东开展药品经营专项检查 及时排查和化解风险隐患 日前,山东省药品监督管理局印发《... -
 国家外汇管理局深化外汇领域改革开放 促进跨境贸易投资便利化 中国人民银行、银保监会、证监会、...
国家外汇管理局深化外汇领域改革开放 促进跨境贸易投资便利化 中国人民银行、银保监会、证监会、... -
 全球气候变化问题日益突出 零碳咖啡见证绿色办会 柜台前排起长龙,咖啡师两手并用,...
全球气候变化问题日益突出 零碳咖啡见证绿色办会 柜台前排起长龙,咖啡师两手并用,... -
 “酸菜味”方便面回归超市货架 方便面市场空间被挤压 近日,多家企业的酸菜味方便面纷纷...
“酸菜味”方便面回归超市货架 方便面市场空间被挤压 近日,多家企业的酸菜味方便面纷纷...
精彩新闻
-
 河南发放转向资金补贴 升级赏花春游产业链 五一将至,春夏之交,全国许多地方...
河南发放转向资金补贴 升级赏花春游产业链 五一将至,春夏之交,全国许多地方... -
 餐饮寒冬季,冰雪时光为何掀起开店热潮? 2020年以来,疫情的阴影一直笼罩着...
餐饮寒冬季,冰雪时光为何掀起开店热潮? 2020年以来,疫情的阴影一直笼罩着... -
 我国消费者权益保护工作面临挑战 加大消费者权益保护力度 中国消费者协会近日在北京发布《中...
我国消费者权益保护工作面临挑战 加大消费者权益保护力度 中国消费者协会近日在北京发布《中... -
 多家银行在个人碳账户方面进行尝试 以零售业务作为主要突破口 个人碳积分达到一定数量,可以用于...
多家银行在个人碳账户方面进行尝试 以零售业务作为主要突破口 个人碳积分达到一定数量,可以用于... -
 个人养老金制度出台 切实保障养老金投资运作安全规范 国务院办公厅近日印发《关于推动个...
个人养老金制度出台 切实保障养老金投资运作安全规范 国务院办公厅近日印发《关于推动个... -
 吉林省畜牧局多措并举 加快推动畜牧企业复工复产 4月25日,记者从吉林省召开的新闻...
吉林省畜牧局多措并举 加快推动畜牧企业复工复产 4月25日,记者从吉林省召开的新闻... -
 交通运输部举行新闻发布会 保持经济运行在合理区间 今天(4月26日),交通运输部举行新...
交通运输部举行新闻发布会 保持经济运行在合理区间 今天(4月26日),交通运输部举行新... -
 直击第53届卡思曼伯意大利博洛尼亚国际美容展!邀您云端逛展 第53届卡思曼伯意大利博洛尼亚国际...
直击第53届卡思曼伯意大利博洛尼亚国际美容展!邀您云端逛展 第53届卡思曼伯意大利博洛尼亚国际... - 盈康生命发布业绩预告,实控人一致行动人增持彰显信心 4月25日,盈康生命科技股份有限公...
-
 学前教育资源结构发生格局性变化 幼儿园“小学化”治理成效显著 教育部今天举行新闻发布会,介绍党...
学前教育资源结构发生格局性变化 幼儿园“小学化”治理成效显著 教育部今天举行新闻发布会,介绍党... -
 多数省份一季度经济运行平稳开局 江西增速领跑 总体来看,大多数省份一季度经济运...
多数省份一季度经济运行平稳开局 江西增速领跑 总体来看,大多数省份一季度经济运... -
 阿卡索优享1v1课程广受赞誉 阿卡索作为一家在英语教育行业拥有...
阿卡索优享1v1课程广受赞誉 阿卡索作为一家在英语教育行业拥有... -
 世界知识产权日 | 天威诚信助力专利证书全面电子化,激发产业创新发展活力 今天,是第22个世界知识产权日。世...
世界知识产权日 | 天威诚信助力专利证书全面电子化,激发产业创新发展活力 今天,是第22个世界知识产权日。世... -
 健康饮食需求激增!DROODS道得富以健康食品助力改善国民健康水平 自健康中国战略实施以来,人民群众...
健康饮食需求激增!DROODS道得富以健康食品助力改善国民健康水平 自健康中国战略实施以来,人民群众... -
 助力疫情期间“不断奶” 达能纽迪希亚守护上海儿童营养 “不掉队” 四月以来,达能纽迪希亚生命早期营...
助力疫情期间“不断奶” 达能纽迪希亚守护上海儿童营养 “不掉队” 四月以来,达能纽迪希亚生命早期营... - 盈康生命发布2021年业绩预告,预计营收首超10亿 4月25日,盈康生命科技股份有限公...
-
 草莓、荔枝、桃花……近100种新口味低度酒在天猫超市开卖 初夏将至,口味新、包装潮的低度酒...
草莓、荔枝、桃花……近100种新口味低度酒在天猫超市开卖 初夏将至,口味新、包装潮的低度酒... -
 戴口罩也能人脸识别 亚略特智能防疫设备落地医院防疫一线 前不久,苹果发布了iOS 15 4,新...
戴口罩也能人脸识别 亚略特智能防疫设备落地医院防疫一线 前不久,苹果发布了iOS 15 4,新... -
 轨道插座是智商税吗?安全好用的MEYEO美沿移动轨道插座,PICK一下! 轨道插座是不是智商税?轨道插座是...
轨道插座是智商税吗?安全好用的MEYEO美沿移动轨道插座,PICK一下! 轨道插座是不是智商税?轨道插座是... -
 电商江湖千帆竞发,卷尾科技助力企业直播带货 短视频应用的兴起,直播成为了当下...
电商江湖千帆竞发,卷尾科技助力企业直播带货 短视频应用的兴起,直播成为了当下... -
 菜鸟正展开街道攻坚战 天猫超市上海配送逐步恢复 上海快递物流恢复情况如何?记者从...
菜鸟正展开街道攻坚战 天猫超市上海配送逐步恢复 上海快递物流恢复情况如何?记者从... -
 Blueglass 自然探索骑行,成为更好的自己 不要忘记去体验伟大不要忘记去致敬...
Blueglass 自然探索骑行,成为更好的自己 不要忘记去体验伟大不要忘记去致敬... -
 2022年五一假期铁路客票预售期是多长时间 自2022年4月7日起,铁路客票预售期...
2022年五一假期铁路客票预售期是多长时间 自2022年4月7日起,铁路客票预售期... -
 5月1日起取消初中毕业后普职分流 让更多人可以升入普通高中 新修订的《中华人民共和国职业教育...
5月1日起取消初中毕业后普职分流 让更多人可以升入普通高中 新修订的《中华人民共和国职业教育... -
 2022年广州从化区幼儿园招生 电脑摇号的比例为招生学位数的90% 非小区配套幼儿园:从化区幼儿园、...
2022年广州从化区幼儿园招生 电脑摇号的比例为招生学位数的90% 非小区配套幼儿园:从化区幼儿园、... -
 常州京城皮肤病医院樊战军:为什么很多皮肤病夜间觉得瘙痒 有皮肤病的友友们有没有觉得很疑惑...
常州京城皮肤病医院樊战军:为什么很多皮肤病夜间觉得瘙痒 有皮肤病的友友们有没有觉得很疑惑... -
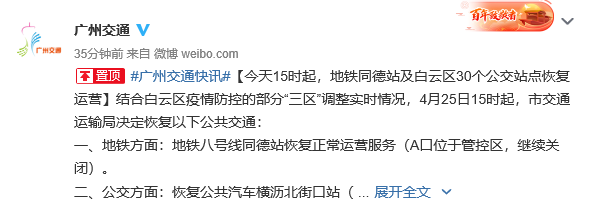 广州地铁8号线同德站B、C口恢复通行 A口位于管控区继续关闭 图源:广州交通微博结合白云区疫情...
广州地铁8号线同德站B、C口恢复通行 A口位于管控区继续关闭 图源:广州交通微博结合白云区疫情... -
 4月25日广州白云区公交站点线路情况一览 结合白云区疫情防控的部分三区调整...
4月25日广州白云区公交站点线路情况一览 结合白云区疫情防控的部分三区调整... -
 新技术“膨体聚四氟乙烯泪沟矫正”在《中国美容医学》成功发表 《中国美容医学》4月2日消息,中日...
新技术“膨体聚四氟乙烯泪沟矫正”在《中国美容医学》成功发表 《中国美容医学》4月2日消息,中日... -
 “膨体聚四氟乙烯泪沟矫正”在《中国美容医学》成功发表 近日,由中日友好医院整形外科副主...
“膨体聚四氟乙烯泪沟矫正”在《中国美容医学》成功发表 近日,由中日友好医院整形外科副主... -
 动起来!与FITURE魔镜见习教练杨舒予一起变身甜酷女孩 近日,国内知名健身镜品牌FITURE魔...
动起来!与FITURE魔镜见习教练杨舒予一起变身甜酷女孩 近日,国内知名健身镜品牌FITURE魔... -
 “书”送甜蜜力量 蜜雪点亮希望 蜜雪冰城总动员为乡村孩子们捐赠图书 2022年4月23日是第27个世界读书日...
“书”送甜蜜力量 蜜雪点亮希望 蜜雪冰城总动员为乡村孩子们捐赠图书 2022年4月23日是第27个世界读书日... -
 吉林加强蓄水工程管理 确保春灌供水安全 4月24日,记者从本轮吉林省疫情防...
吉林加强蓄水工程管理 确保春灌供水安全 4月24日,记者从本轮吉林省疫情防... -
 山东开展药品经营专项检查 及时排查和化解风险隐患 日前,山东省药品监督管理局印发《...
山东开展药品经营专项检查 及时排查和化解风险隐患 日前,山东省药品监督管理局印发《... -
 国家外汇管理局深化外汇领域改革开放 促进跨境贸易投资便利化 中国人民银行、银保监会、证监会、...
国家外汇管理局深化外汇领域改革开放 促进跨境贸易投资便利化 中国人民银行、银保监会、证监会、... -
 全球气候变化问题日益突出 零碳咖啡见证绿色办会 柜台前排起长龙,咖啡师两手并用,...
全球气候变化问题日益突出 零碳咖啡见证绿色办会 柜台前排起长龙,咖啡师两手并用,... -
 “酸菜味”方便面回归超市货架 方便面市场空间被挤压 近日,多家企业的酸菜味方便面纷纷...
“酸菜味”方便面回归超市货架 方便面市场空间被挤压 近日,多家企业的酸菜味方便面纷纷... -
 人民银行将普惠小微企业贷款延期支持工具转换为支持工具 记者从人民银行广州分行获悉,近日...
人民银行将普惠小微企业贷款延期支持工具转换为支持工具 记者从人民银行广州分行获悉,近日... -
 北京商超通过产地直采调货机制紧急增加货量 保障市场供应稳定 面对突发的疫情,北京各大商超企业...
北京商超通过产地直采调货机制紧急增加货量 保障市场供应稳定 面对突发的疫情,北京各大商超企业... -
 农村“一刻钟”建模 一体化县域商业网络体系升级 北京的便民商业网点建设已从市区延...
农村“一刻钟”建模 一体化县域商业网络体系升级 北京的便民商业网点建设已从市区延... -
 百万医疗险0免赔额产品面世 缓解小额医疗费用无法理赔痛点 几百元的保费、上百万元的保额,百...
百万医疗险0免赔额产品面世 缓解小额医疗费用无法理赔痛点 几百元的保费、上百万元的保额,百... -
 步步高披露2021年业绩预告 净利润同比由盈转亏 4月25日,步步高(002251)一字跌停...
步步高披露2021年业绩预告 净利润同比由盈转亏 4月25日,步步高(002251)一字跌停... -
 资金掮客卷土重来 做起了“过桥”融资的生意 受疫情多地散发影响,部分用户因确...
资金掮客卷土重来 做起了“过桥”融资的生意 受疫情多地散发影响,部分用户因确... -
 辛巴再陷“假货”风波 到底谁才是“正品”? 主播辛巴再陷假货风波,辛巴与涉事...
辛巴再陷“假货”风波 到底谁才是“正品”? 主播辛巴再陷假货风波,辛巴与涉事... -
 自动驾驶是场马拉松 资本明显往头部企业聚集 这块碳是我和团队调研矿山时捡回来...
自动驾驶是场马拉松 资本明显往头部企业聚集 这块碳是我和团队调研矿山时捡回来... -
 潍坊高新区通过工业地产模式建设动力装备国际配套产业园 产业是城市发展的基石,优化其生态...
潍坊高新区通过工业地产模式建设动力装备国际配套产业园 产业是城市发展的基石,优化其生态... -
 国内咖啡豆市场持续火爆 保税仓储业务减少关税成本等资金占用 日前,在办结海关监管通关手续后,...
国内咖啡豆市场持续火爆 保税仓储业务减少关税成本等资金占用 日前,在办结海关监管通关手续后,... -
 辽宁省持续优化口岸营商环境 为市场主体提供通关预期 2022年以来,辽宁省坚决贯彻党中央...
辽宁省持续优化口岸营商环境 为市场主体提供通关预期 2022年以来,辽宁省坚决贯彻党中央... -
 我国冷链物流行业高质量发展 布局建设骨干冷链物流基地 近日,交通运输部、国家铁路局、中...
我国冷链物流行业高质量发展 布局建设骨干冷链物流基地 近日,交通运输部、国家铁路局、中... -
 江苏省依托广交会产业帮扶优势 帮助特色产业对接大市场 走过六十五载的中国第一展,除了作...
江苏省依托广交会产业帮扶优势 帮助特色产业对接大市场 走过六十五载的中国第一展,除了作...